Senyawa yang terbentuk dari dua atau lebih unsur non logam seperti karbon dan hidrogen yang disebut senyawa kovalen. Naoh koh na₂so₄ aloh₃ kclo₄.
Pengertian Ikatan Ion Syarat Ciri Sifat Pembentukan Contoh
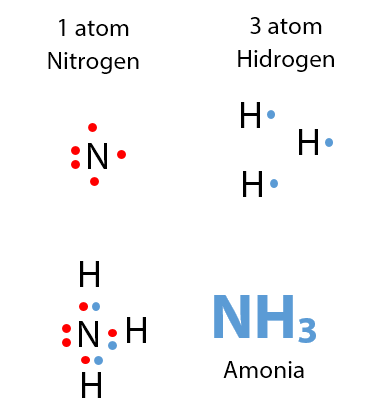
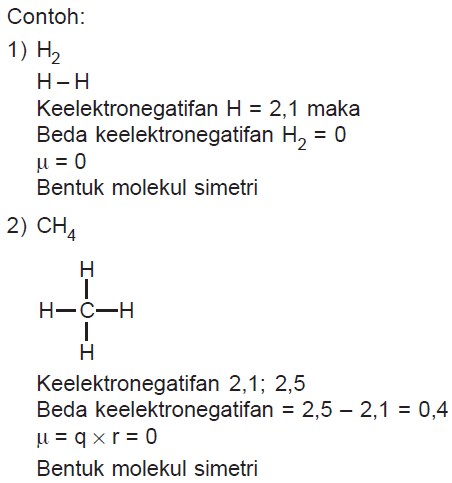
Contoh senyawa ion dan kovalen. Hal ini disebabkan senyawa kovalen polar mengandung ion ion jika dilarutkan dalam air dan senyawa tersebut temasuk senyawa elektrolit lemah. Ini adalah ikatan kimia dengan atom berbagi elektron valensi. Sifat senyawa ion maupun sifat senyawa kovalen dapat kita jabarkan sebagai berikut. Meskipun mereka terdiri dari ion bermuatan positif dan negatif senyawa ion netral secara elektrik karena muatannya selalu sama dan berlawanan. Metana adalah contoh dari senyawa kovalen. Semua yang ada di dunia ini memiliki sifat sifatnya masing masing.
Contoh tambahan senyawa yang mengandung ikatan ion dan kovalen sekaligus. Mereka juga memiliki sifatnya sendiri sehingga bisa menjadi pembeda dengan senyawa yang lain. Meski demikian senyawa kovalen dan ionik memiliki beberapa perbedaan dalam menghantarkan arus listrik. Selain contoh contoh ikatan ion mungkin bermanfaat untuk mengetahui contoh contoh senyawa yang mengandung ikatan kovalen dan juga senyawa yang mengandung ikatan kimia ion dan kovalen. Dan salam chemistry. Ketiga jenis senyawa kimia ini tentunya sangatlah penting untuk kita pelajari karena pada materi materi kimia tingkat atas yang akan adik adik pelajari berikutnya akan selalu berkaitan dengan konsep.
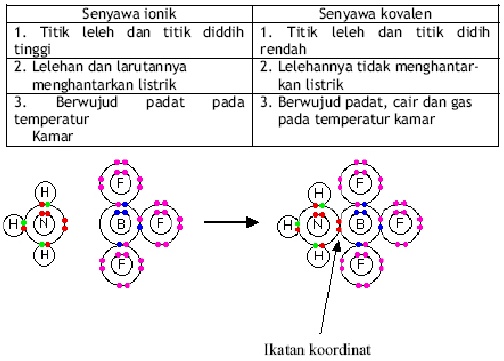
Sebagai contoh amonium klorida memiliki ikatan ion antara ion poliatomik nh 4 dan ion cl tetapi di dalam ion amonium atom nitrogen dan hidrogen dihubungkan oleh ikatan kovalen. Jadi pada contoh tambahan ini kita dapat melihat bahwa baik ikatan ion maupun kovalen terdapat di dalamnya karena terdapat atom unsur logam dan lebih dari satu atom unsur non logam. Senyawa kovalen juga dikenal sebagai senyawa molekuler. Sebagai besar senyawa senyawa yang dapat membentuk ikatan ion juga memiliki struktur yang keras dan juga mudah patah sementara dalam senyawa kovalen umumnya lebih lunak. Pada umumnya senyawa kovalen pada berbagai wujud tidak dapat menghantar arus listrik atau bersifat non elektrolit kecuali senyawa kovalen polar. Seperti yang juga adik adik ketahui bahwa senyawa kimia terutama senyawa kimia anorganik itu terdiri dari 3 jenis senyawa yaitu senyawa ion senyawa kovalen polar dan senyawa kovalen non polar.
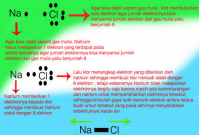
Ini adalah contoh ikatan kovalen dan senyawa kovalen. Dalam senyawa kovalen atom dari unsur unsur yang berbeda ada di dalam molekul oleh ikatan kovalen. Begitu juga dengan senyawa ion dan kovalen. Kepolaran dan kelarutannya ikatan ion yang terbentuk melalui ikatan antara ion positif dan ion negative ini menyebabkan senyawa yang dihasilkan dari ikatan yang disebut juga dengan nama homopolar ini bersifat polar. Contoh senyawa kovalen non polar h2 n2 cl2 br2 i2 ch4 ccl4 bcl3 no2 sf6 bf3 co2 dll ok beitulah penjelasan mas dennis mengenai pengertiansifat dan contoh dari senyawa kovalen. Semoga artikel ini dapat membantu dan menambah wawasan sobat semuanya.
Perbedaan senyawa ionik dan senyawa kovalen pengertian contoh reaksi kimia kemampuan untuk menghantarkan arus listrik tidak hanya dimiliki oleh senyawa ionikbeberapa senyawa kovalen juga mampu menghantarkan listrik.