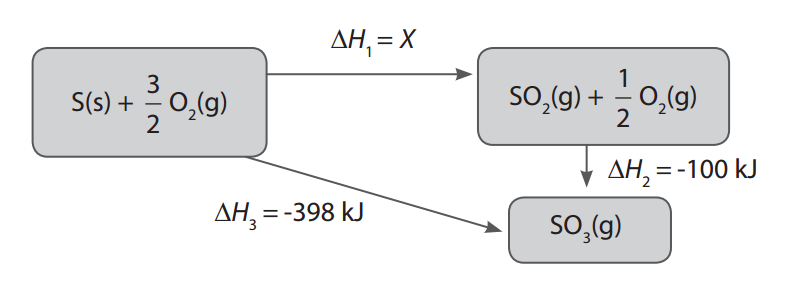
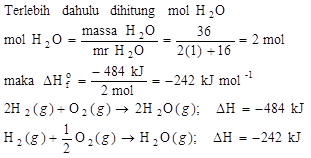A r h 1 a r o 16. Contoh soal tentang kalor.

Pembahasan Soal Termokimia Sbmptn Kimia 2013 Kode Soal 333
Contoh soal dan jawaban persamaan termokimia. 2h2g o2g 2h2o l δh 572 kj tuliskan persamaan termokimia untuk pembentukan satu mol air. Sistem adalah segala sesuatu yang menjadi pusat perhatian sedangkan lingkungan yaitu hal hal di luar sistem yang membatasi sistem dan dapat mempengaruhi sistem. Soal no1 jelaskan pengertian sistem dan lingkungan. Contoh soal termokimia pembahasan jawaban kelas 11 soal essay termokimia. Persamaan reaksi termokimianya menjadi. H 2 g ⅟ 2 o 2 g h 2 0ℓ h 28585 kjmol.
Untuk suatu persamaan reaksi dengan semua zat di ketahui harga hf nya masing masing. Diketahui entalpi pembentukan standar h f h 2 0ℓ 28585 kjmol. Jika koefisien persamaan pelelehan es digandakan dua kalinya perubahan entalpinya juga dikalikan dua. Contoh soal termokimia pilihan ganda dan pembahasannya bagian dari ilmu kimia yang mempelajari perubahan kalor atau panas suatu zat yang menyertai suatu reaksi atau proses kimia dan fisika disebut termokimiasecara operasional termokimia berkaitan dengan pengukuran dan pernafsiran perubahan kalor yang menyertai reaksi kimia perubahan keadaan dan pembentukan larutan. Tuliskan juga reaksi untuk kebalikannya. Ah f h 2 0ℓ 28585 kjmol persamaan termokimia reaksi pembentukan h20.
Soal termokimia pilihan ganda dan pembahasannya. Pada reaksi antara air panas dengan gula yang menyebabkan gelas menjadi panas merupakan contoh dari reaksi eksoterm. 2h 2 g o 2 g 2h 2 og δh 4836 kj. Contoh soal reaksi eksoterm dan endoterm. Persamaan termokimia dan entalpi. Contoh soal dan jawaban persamaan termokimia.
Soal dan jawaban termokimia 1 diketahui persamaan termokimia sebagai berikut. Latihan soal termokimia 40 soal dan pembahasan. Unit pembangkit uap air di pabrik dinamakan. Pengertian persamaan reaksi rumus dan contoh soal tahukah anda apa yang dimaksud dengan termokimia. Berapakah kalor yang diperlukan untuk menguraikan 13 gram air menjadi hidrogen dan oksigen pada keadaan standar. Sebanyak 2 mol h2g dan 1 mol o2g bereaksi membentuk air disertai pelepasan kalor sebesar 572 kj.
Pembentukan satu mol air berarti mengalikan persamaan termokimia dengan faktor. Persamaan termokimia adalah persaman reaksi setara yang menyertakan kalor reaksi entalpi reaksi yang menunjukkan hubungan antara massa dan energi. 2h 2 os 2h20ℓ δh 601 kjmol. Karena disini akan mengulas tentang pengertian termokimia sistem termokimia dan rumus termokimia beserta contohnya secara lengkap.